
Monitoring glioblastoma extracellular vesicle evolution using a nanodiagnostic platform to detect glioma stem cells driving recurrent disease
利用纳米诊断平台监测胶质母细胞瘤细胞外囊泡的演变以检测驱动疾病复发的胶质瘤干细胞
论文信息:Zhang, Z., Lobb, R. J., Tooney, P., Wang, J., Lane, R., Zhou, Q., Niu, X., Faulkner, S., Al-Iedani, O., Day, B. W., Puttick, S., Rose, S., Fay, M., & Trau, M. (2026). Monitoring glioblastoma extracellular vesicle evolution using a nanodiagnostic platform to detect glioma stem cells driving recurrent disease. Science advances, 12(5), eadt2804. https://doi.org/10.1126/sciadv.adt2804
主讲人:张梓桐,2026年3月29日
研究进展 or 研究背景:
胶质母细胞瘤(GBM)是一种起源于中枢神经系统(CNS)的侵袭性强、转移性高的原发性脑肿瘤。其预后极差,中位生存期约为 14 个月。治疗耐药性的快速产生和局部频繁复发是导致患者预后不良的关键特征。胶质母细胞瘤肿瘤进展的准确监测难度大、成本高,目前主要依赖磁共振成像(MRI)等影像学手段。胶质母细胞瘤临床管理中的标准诊断方法(即切除标本的组织病理学检查)仅能提供肿瘤有限的时间分子谱信息,无法动态监测肿瘤进展。此外,MRI 检测肿瘤进展的早期迹象也存在挑战,因为放疗后3个月内的假性进展和放疗后 3-12 个月的放射性坏死,会导致诊断结果的解读变得复杂。因此,开发治疗期间监测肿瘤演变的无创方法,对于指导这一恶性肿瘤的治疗管理至关重要。
近年来,液体活检作为一种诊断手段应运而生,可通过分析患者血液中的肿瘤特征,实现肿瘤分型、预后监测和治疗反应评估。这些无创方法能够通过血液样本反映肿瘤的分子特征。作为液体活检标志物,外泌体或小细胞外囊泡(sEV)是细胞释放的纳米级囊泡(直径 50-150 nm)。这类囊泡是细胞间通讯的关键介质,携带蛋白质、核酸、代谢物和脂质等分子物质。最重要的是,多项研究表明,胶质母细胞瘤肿瘤释放的小细胞外囊泡能够穿过完整的血脑屏障(BBB)进入外周血。部分研究发现,与健康对照者相比,胶质母细胞瘤患者体内总小细胞外囊泡浓度整体升高,且原发肿瘤经有效治疗后,囊泡负荷明显降低。但也有研究表明,全身总小细胞外囊泡浓度升高并非胶质母细胞瘤特有的现象,这意味着仅以囊泡浓度作为检测指标可能并不适用。进一步研究证实,小细胞外囊泡能够反映胶质母细胞瘤原发肿瘤的分子谱,并及时为治疗方案的制定提供临床信息,这为将胶质母细胞瘤小细胞外囊泡作为指导临床管理决策的工具提供了可能。
胶质母细胞瘤小细胞外囊泡的研究进展受限于一个关键难题:难以从血液中的非靶标总小细胞外囊泡中特异性分离和鉴定胶质母细胞瘤来源的小细胞外囊泡。以往研究曾尝试筛选与循环胶质母细胞瘤小细胞外囊泡相关的特异性蛋白成分,包括跨膜 L1 细胞黏附分子、表皮生长因子受体变体 III(EGFRvIII)、血管性血友病因子和多配体蛋白聚糖-1。然而,这些生物标志物也在多种正常组织中表达,无法实现胶质母细胞瘤小细胞外囊泡的特异性分离。为解决胶质母细胞瘤组织来源小细胞外囊泡检测缺乏特异性的问题,作者在血液中的小细胞外囊泡上鉴定出了独特的胶质母细胞瘤特征。通过将胶质母细胞瘤小细胞外囊泡特征与纳米剪切多重表面增强拉曼光谱(SERS)平台(命名为胶质母细胞瘤细胞外囊泡监测表型分析芯片,GEMPAC)相结合,作者实现了对胶质母细胞瘤患者小细胞外囊泡表面蛋白组成的高灵敏度、高精度谱分析。
解决方案 or 研究内容:
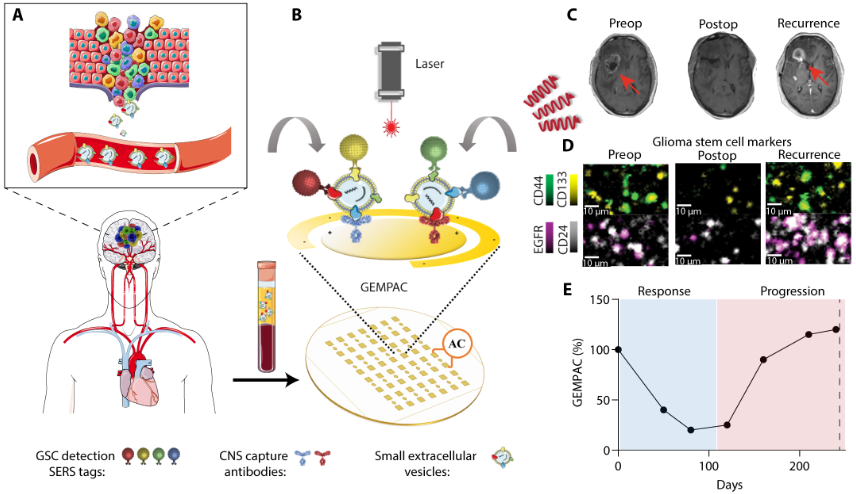
本研究中,GEMPAC检测芯片通过靶向由跨膜蛋白钠/钾转运ATP酶β2亚基(ATP1B2)和兴奋性氨基酸转运体2(EAAT2)组成的独特中枢神经系统特征,精准捕获胶质母细胞瘤小细胞外囊泡;这两种蛋白在正常中枢神经系统和胶质母细胞瘤组织中均高表达。作者通过检测胶质瘤干细胞(GSC)标志物,对捕获的中枢神经系统小细胞外囊泡的恶性表型进行谱分析,以发现可能驱动疾病复发和治疗耐药的胶质瘤干细胞亚群。此前的单细胞RNA测序(scRNA-seq)数据揭示了表征胶质瘤干细胞类细胞状态的多种表面标志物:其中,CD24在神经祖细胞样(NPC样)细胞中高表达,CD44在间充质细胞样(MES样)细胞中高表达,CD133 在少突胶质前体细胞样(OPC样)细胞中高表达,EGFR 在星形胶质细胞样(AC样)细胞中高表达。作者利用 GEMPAC 平台捕获胶质母细胞瘤小细胞外囊泡,并监测患者治疗前后胶质瘤干细胞亚群的演变。令人振奋的是,通过分析治疗期间胶质瘤干细胞亚群的变化,作者成功检测到患者的治疗反应和肿瘤进展,为胶质母细胞瘤的临床管理提供了新的思路。作者认为,这一诊断平台有望通过监测循环中与胶质母细胞瘤胶质瘤干细胞相关的小细胞外囊泡,为未来的治疗提供支持,优化临床决策,从而提高患者的生存率。
要点:
1.本研究开发了GEMPAC纳米平台,通过检测血液中GBM来源小细胞外囊泡的六种标志物(CNS捕获标志物ATP1B2、EAAT2;GSC状态标志物CD24、CD44、CD133、EGFR),动态监测肿瘤演变。术后GEMPAC评分可预测生存,并能提前预警复发,反映治疗压力下的克隆选择。
总结与展望:
本研究证明,GEMPAC平台能够通过分析血浆中GBM来源sEVs的GSC标志物,实现肿瘤演变的非侵入式动态监测。该技术克服了影像学无法反映分子变化的局限,可在复发前预警、评估治疗响应、揭示靶向治疗诱导的表型转换(如EGFR靶向治疗后CD44上升)。GEMPAC评分在术后具有独立预后价值,且适用于多种治疗方案,展现出良好的临床转化潜力。未来需在更大规模队列中验证其预测效能,并推动检测流程的标准化与自动化。将GEMPAC与单细胞测序等技术整合,有望进一步细化患者分层,指导个体化治疗,并为其他脑部疾病的液体活检提供新范式。

